Neurol Neuroimmunol Neuroinflamm. 2015 Jun; 2 (3): E98.
Efecto positivo de la dexametasona liberada desde eritrocitos en la ataxia-telangiectasia
Vincenzo Leuzzi , MD,
Roberto Micheli , MD,
Daniela D'Agnano , MD,
Anna Molinaro , PT,
Tulia Venturi , PT,
Alessandro Plebani , MD,
Annarosa Soresina , MD,
Mirella Marini , MD,
Pierino FERREMI Leali , MD,
Isabella Quinti , MD,
María C. Pietrogrande , MD,
Andrea Finocchi , MD,
Elisa Fazzi , MD,
Luciana Chessa , MD, y
Mauro Magnani , MD

Este artículo ha sido
citado por otros artículos en PMC.
Abstracto
Objetivo:
La ataxia-telangiectasia (AT) es una enfermedad neurodegenerativa rara, devastadora que presentan ataxia-aparición temprana, telangiectasia oculocutáneo, inmunodeficiencia, radiosensibilidad, y la propensión al cáncer. En un estudio previo de fase 2, se demostró que 6 infusiones mensuales de eritrocitos autólogos cargados con dexametasona (EryDex; EryDel, Urbino, Italia) fueron eficaces en la mejora de deterioro neurológico en pacientes jóvenes con AT. El presente artículo presenta los resultados de la extensión de este estudio por un período adicional de 24 meses.
métodos:
Después del final de la primera prueba, 4 pacientes continuaron recibiendo tratamiento con infusiones mensuales EryDex durante 24 meses adicionales, y su resultado clínico se comparó con el de 7 pacientes de la misma edad que dejaron el tratamiento después de los primeros 6 infusiones. El protocolo incluyó la evaluación en serie de la ataxia (por International Cooperative Ataxia Rating Scale) y la conducta adaptativa (por Adaptive Behavior Scales Vineland) y las pruebas clínicas y de laboratorio que revelan efectos adversos tratados previamente y dependientes de esteroides, si está presente.
resultados:
Los pacientes en el estudio ampliado experimentaron una mejoría neurológica continua con respecto a su estado de pretratamiento, mientras que los controles mostraron un deterioro neurológico progresivo (de acuerdo con la historia natural de la enfermedad) después de la interrupción del tratamiento. El sistema de suministro que adoptamos demostrado ser seguro y bien tolerado y no se observaron ninguno de los efectos secundarios generalmente asociados con la administración crónica de corticosteroides durante todo el juicio.
conclusiones:
Estos resultados preliminares prometedores exigen un estudio controlado a gran escala en el tratamiento prolongado de pacientes con AT con eritrocitos cargados con dexametasona.
La ataxia-telangiectasia (AT) es una enfermedad genética rara 1 , 2 causada por mutaciones en el ataxia telangiectasia mutada ( ATM gen), lo que resulta en una enfermedad multisistémica que se presentan con ataxia de aparición temprana, teleangiectasias OCULOCUTÁNEO, oftalmoplejía supranuclear progresiva, inmunodeficiencia, recurrente infecciones sinopulmonares, radiosensibilidad y la propensión al cáncer. En la forma clásica, los pacientes están adaptadas para personas dependientes de la edad de 10 años, 1 y su esperanza de vida es de aproximadamente 25 años. 1 , 2 No existe una terapia efectiva modificadora de la enfermedad es actualmente disponible.
Los estudios observacionales han sugerido que la betametasona puede ser eficaz en la mejora de las funciones neurológicas en pacientes con. EN 3 , 4 Un ensayo controlado a corto plazo confirmó la eficacia de betametasona oral (0,1 mg / kg), 5 pero los efectos secundarios de los corticosteroides se observaron rápidamente. Para superar estos efectos secundarios y explorar los efectos de un tratamiento más prolongado en el resultado neurológico, se realizó recientemente un ensayo de un solo brazo, de etiqueta abierta, de 6 meses extendió la fase 2 en el que los pacientes que participaron recibieron un tratamiento mensual de 50 ml de eritrocitos autólogos cargados con 2 viales de 250 mg de fosfato de dexametasona (DSP) por EryDex (EryDel, Urbino, Italia) procedimiento. 6 de manera similar a la betametasona, dexametasona tiene una potencia anti-inflamatoria alta y carece de actividad mineralocorticoides. DSP es convertida a la dexametasona por fosfatasas eritrocitos 'y se libera en el torrente sanguíneo durante unos 20-30 días. 7
Después de 6 infusiones, los pacientes experimentaron una mejoría clínica de alrededor de 5 puntos en la Clasificación Cooperative Ataxia Escala Internacional (ICARS) 8 y una mejora significativa en el comportamiento de adaptación, evaluada por Escalas de Comportamiento Vineland Adaptive (VABS), 9sin la aparición de dependiente de esteroides eventos adversos. La mejora fue más relevante en pacientes con deterioro neurológico menos grave y se vio afectada por la eficiencia del procedimiento DSP de carga en los eritrocitos. 6 Se presentan los resultados de la extensión de este estudio preliminar para un período adicional de 24 meses.
MÉTODOS
Al final de la primera prueba de 6 meses, 6 4 pacientes varones (edad media de 10,6 años; SD 2,8 años, rango 8.7-14.2 años) solicitó y fueron autorizados por el Comité de Ética para continuar el tratamiento EryDex. Hasta el momento han sido tratados mensual por un período adicional de 24 meses. Los ICARS y VABS puntuaciones de los pacientes en el estudio prolongado antes del inicio del tratamiento y después de 6 y 24 infusiones EryDex se compararon con los de los 7 pacientes con AT (2 hombres, 5 mujeres; media de edad de 11,8 años; SD 3,5 años ;. rango 8.2-19.2 años) que se detuvo el tratamiento después de la sexta infusión, como estaba previsto originalmente por el diseño del estudio 6 de acuerdo con una cláusula de medicamentos de uso compasivo, la selección de los continuadores se basó en la decisión de los padres (es decir, sin criterio de inclusión externa podría aplicarse), y se seleccionaron los controles entre los que abandonaron al tratar de ajustarse mejor a las características clínicas de los continuadores ( ).Durante el estudio de extensión, el procedimiento de carga se ha optimizado aún más por la obtención de un DSP encapsulado de 9,4 ± 0,8 mg / bolsa (frente a 6,7 ± 6,9 en el estudio previo 6 ) con la misma dosis del medicamento. La evaluación también incluyó pruebas clínicas y de laboratorio destinados a detectar tratamiento-y los efectos adversos dependientes de esteroides.
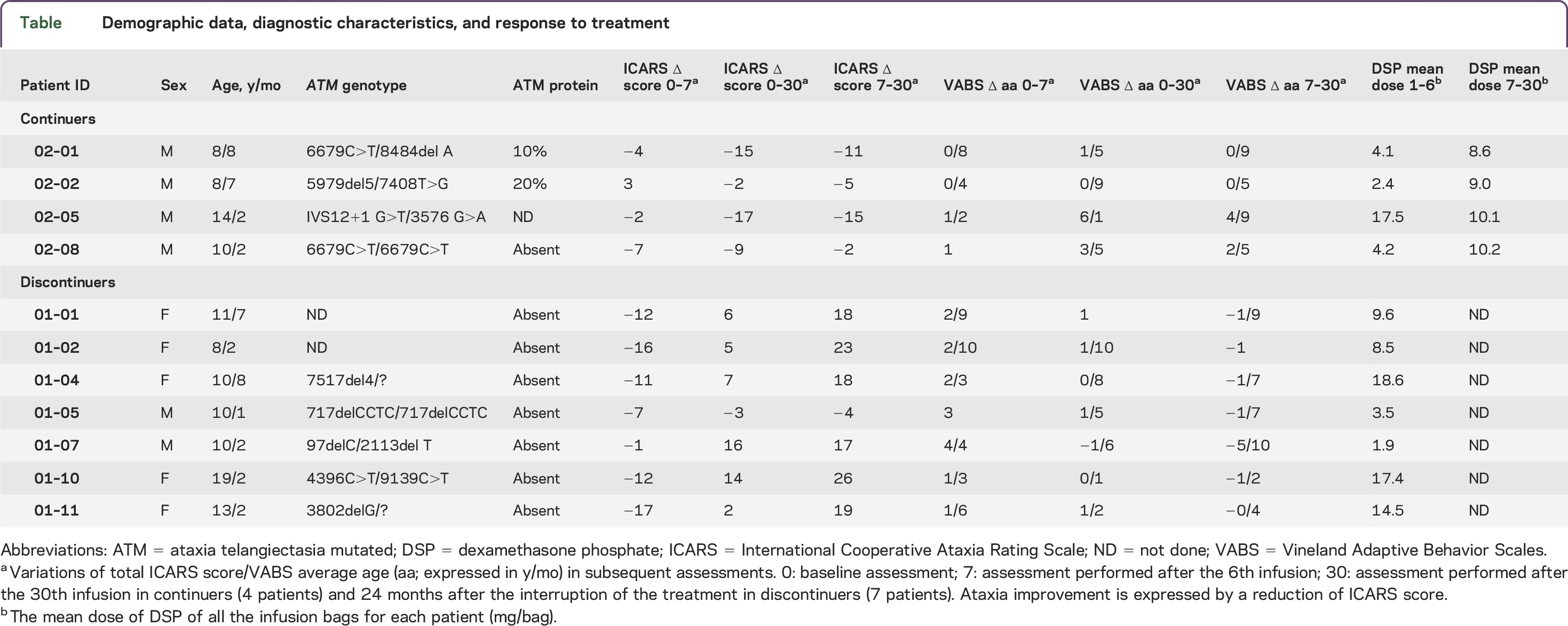
Table
Demographic data, diagnostic characteristics, and response to treatment
aprobaciones estándar de protocolo, registros y autorizaciones de los pacientes.
La ampliación fue autorizada por el Comité de Ética. Current Controlled Trial registro 2010-022315-19SpA.
RESULTADOS
La resume la respuesta clínica al tratamiento al final de los primeros 6 meses (11 pacientes) y después de 24 meses más en continuadores (4 pacientes masculinos) y abandonan (7 pacientes; 2 varones, 5 mujeres). También se muestra la incorporación media DSP durante ambos los ensayos originales y extendidas. Al final de la primera prueba de 6 meses, y ICARS Vabs decenas de continuadores y abandonan eran ICARS 52.2 ± 7.1 vs 43 ± 2.9 y VABS 6 ± 2,3 vs 8,2 ± 0,6, respectivamente.
Después de 30 meses, los pacientes en el estudio prolongado experimentaron una mejoría en la puntuación ICARS de 10,7 puntos (SD 6,75; intervalo 2-17) con respecto a la puntuación obtenida en la evaluación clínica basal. Por el contrario, los ICARS puntuación de los 7 pacientes que interrumpieron el tratamiento empeorado en 6,7 puntos (SD 6,5; intervalo de 3-16 +) (Mann-Whitney U = 1,00; z = 2,45; p = 0,013803).Por otra parte, todos los continuadores y sólo 1 de cada 7 abandonan mejoraron sus ICARS puntuación (prueba exacta de Fisher, p = 0,0152). En consecuencia, Vabs edad promedio mejoró en 2,10 años (DE 2,4 años, rango 9 meses-6,1 años) y de 0,9 años (SD 1 año, rango de -1.6 a 1,10 años) en continuadores y abandonan, respectivamente (Mann-Whitney U = 5,50; z = 1,60; p = 0,10). Por otra parte, ICARS puntuaciones al final de la primera prueba de 6 meses y 30 meses después de la mejora en 8,2 puntos (DE 5,8, rango 2-17) en los continuadores y agravadas por 17,8 puntos (SD 6.9, rango de -4 a 26) en los que abandonaron (Mann-Whitney U = 0,00; z = 2,64; p = 0,008). La ataxia mejoró en 4 de 4 continuadores y en 1 de 7 abandonan (prueba exacta de Fisher, p = 0,015) ( ). Variaciones concomitantes en VABS entre los continuadores y que abandonaron fueron 2,6 años (DE 2,3 años, rango 0.5-4.9 años) y -1.7 años (DE 11 meses; rango -4 meses +2,9 años), respectivamente (Mann-Whitney U = 0,00; z = 2,64; p = 0,008).
Figure
Neurologic impairment variation and duration of the treatment in patients with ataxia-telangiectasia
variación deterioro neurológico y la duración del tratamiento en pacientes con ataxia-telangiectasia
La tendencia de la Clasificación Cooperativa Ataxia Escala Internacional (ICARS) puntuación variaciones (con SD) en 4 pacientes con ataxia-telangiectasia que fueron tratados durante 30 meses con infusiones mensuales de eritrocitos cargados con dexametasona fosfato autólogo en comparación con los ICARS decenas de 7 pacientes que interrumpieron el tratamiento después de los primeros 6 infusiones mensuales. 0 (línea de base), 7 (después de los primeros 6 infusiones), y 30 (después de 30 meses) representan los puntos de tiempo programados para las evaluaciones posteriores. En continuadores, 30 es también el número total de infusiones antes de la última evaluación. En el rojo es el juicio común (0-7) de los 11 pacientes, en azul son las variaciones en la puntuación ICARS 4 continuadores (0-30; 7-30), y en verde son las variaciones en la puntuación ICARS 7 abandonan (0- 30; 7-30). El aumento de la puntuación refleja el empeoramiento de la ataxia.
No se observaron reacciones adversas dependientes de esteroides durante todo el período de tratamiento.Las pruebas estándar de laboratorio, examen físico, signos vitales y ECG fueron normales. Los parámetros adicionales de laboratorio, tales como el colesterol (lipoproteína de alta densidad total de, y la lipoproteína de baja densidad), la hemoglobina glicosilada (HbA1c), y la sangre y el cortisol urinario estaban dentro del rango normal. CD4 + recuento de linfocitos se mantuvo estable durante el período de tratamiento, pero por debajo del rango normal para 3 de los 4 pacientes. Α-fetoproteína niveles sanguíneos aumentaron en todos los pacientes, independientemente del tratamiento que se sometieron.
DISCUSIÓN
La administración de corticosteroides a largo plazo es eficaz para retrasar la progresión de la distrofia muscular de Duchenne. 10 Recientemente hemos informado de una mejora estadísticamente significativa en los síntomas atáxicos con células rojas DSP-cargada en una cohorte de pacientes jóvenes con AT. 6 A pesar de este nuevo tratamiento no tuvo los efectos secundarios comunes del tratamiento crónico con esteroides, fue aparentemente menos efectivos tratamiento betametasona continuación, oral, lo que resultó en una mejora media de 13 puntos sobre los ICARS después de un mes de tratamiento. 5 los datos actuales son más alentadores, lo que demuestra que después de 30 meses de tratamiento de los pacientes experimentaron una mejora de 10,7 puntos en ICARS puntuación media y 3 años de edad promedio VABS con respecto a su estado basal. Por el contrario, los ICARS puntuación de los que abandonaron a los 30 meses había empeorado en 6,7 puntos y la media de edad VABS había mejorado sólo 0.9 años. La brecha de 26 puntos entre ICARS continuadores y abandonan a los 30 meses con respecto a la puntuación obtenida por los 2 grupos después de los primeros 6 meses de tratamiento es un hallazgo importante.
Aunque preliminares, los presentes resultados son importantes: 2,5 años es un lapso de tiempo suficiente como para revelar el deterioro neurológico progresivo que caracteriza a la historia clínica natural de AT. 1 ,2 El hecho de que los que abandonaron experimentaron una disminución de sus condiciones neurológicas vez que los esteroides eran interrumpida sugeriría un efecto sintomático del tratamiento en lugar de un cambio de plástico que implica el mecanismo patogénico básico de la enfermedad. De lo contrario, la mejoría clínica persistente se observó hasta ahora en los continuadores conflictos con esta hipótesis.
Varias limitaciones metodológicas (falta de cegamiento y el placebo en el tratamiento de la asignación, el tamaño pequeño de la muestra, la falta de criterios clínicos para la inscripción de pacientes externos) afectan a nuestro estudio, que se basa en una observación empírica post hoc. La falta de escalas de calificación dedicados-AT es una limitación metodológica más intrínseca. Sin embargo, en la cara de una enfermedad tan dramática, intratable, cualquier observación clínica sugiere un posible tratamiento merece ser considerado.
Cualquiera que sea el efecto biológico de los esteroides en el AT, los datos actuales apoyan la idea de que un tratamiento prolongado puede retrasar y quizás desviar el curso natural de la enfermedad. Por otra parte, el sistema de entrega adoptamos fue confirmado para ser seguro y bien tolerado, ya que después de este período prolongado de tiempo no se pudieron detectar efectos secundarios. Un estudio controlado a gran escala sobre el tratamiento con esteroides prolongada por DSP cargado en los eritrocitos en pacientes con AT es obligatoria con el fin de verificar estos datos preliminares.
RECONOCIMIENTO
Los autores agradecen a los Dres. L. Buccone, C. Pignata, F. Specchia, y A. Trizzino por referir a los pacientes; las asociaciones (Amici di Valentina, Noi por Lorenzo, AISA, AIP) que ayudaron a las familias en sus desplazamientos y estancias en Roma o Brescia; todos el personal del hospital (médicos, enfermeras, fisioterapeutas, técnicos, etc.); y la EryDel patrocinador para prestar ayuda económica y el sistema EryDex.
GLOSARIO
| A |
la ataxia-telangiectasia |
| Cajero automático |
ataxia telangiectasia mutada |
| DSP |
fosfato de dexametasona |
| ICARS |
Escala Internacional Cooperativa Ataxia |
| VABS |
Escala de Comportamiento Vineland Adaptive |
CONTRIBUCIONES DE AUTOR
Todos los autores han hecho una contribución sustancial para tener derecho a la autoría. Cada autor que aparece en el manuscrito ha visto y aprobado la presentación de esta versión del manuscrito y asume plena responsabilidad por el manuscrito. Vincenzo Leuzzi: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, adquisición de datos. Roberto Micheli: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, adquisición de datos. Daniela D'Agnano: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, adquisición de datos. Anna Molinaro: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, análisis e interpretación de los patrones de neuromotoras de los pacientes. Tullia Venturi: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, análisis e interpretación de los patrones de neuromotoras de los pacientes. Alessandro Plebani: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Annarosa Soresina: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Mirella Marini: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Pierino FERREMI Leali: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Isabella Quinti: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos.María C. Pietrogrande: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Andrea Finocchi: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos. Elisa Fazzi: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, análisis e interpretación de los patrones de neuromotoras de los pacientes. Luciana Chessa: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, la interpretación de análisis molecular. Mauro Magnani: redacción / revisión del manuscrito, el análisis y la interpretación de los datos clínicos y bioquímicos, adquisición de datos.
financiación del estudio
EryDel proporcionó apoyo económico y el Sistema EryDex.
REVELACIÓN
V. Leuzzi, R. Micheli, D. D'Agnano, A. Molinaro, T. Venturi, A. Plebani, A. Soresina, M. Marini, y PF Leali reportan ninguna otra declaración. I. Quinti está en la junta de asesoramiento científico para CSL Behring, es miembro del consejo editorial de Frontiers in Immunology , y recibió apoyo para investigación de Jeffrey Modell Foundation. MC Pietrogrande reporta ninguna otra declaración. A. Finocchi recibido apoyo para investigación de Ministerio de Salud de Italia. E. Fazzi y L. Chessa reportan ninguna otra declaración. M. Magnani es el CSO de EryDel SpA, posee una patente para la encapsulación de agentes dentro de los eritrocitos, recibió apoyo para investigación de la Fundación Caja de Ahorros de Fano, y participa en el capital EryDel SpA. Ir a Neurology.org/nn para las formas de revelación completa.
Referencias
1. Sedgwick O, E. Boder Ataxia-teleangiectasia . En: Vinken PJ, Bruyn GW, editores. ., Editores Manual de Neurología clínica . Vol 14 Amsterdam: Elsevier; 1972: 267-239.
2.
La ataxia-teleangiectasia; AT, # 208900. Herencia mendeliana en el hombre (MIM), Centro de Genética Médica, Universidad John Hopkins, Baltimore, MD, y el Centro Nacional de Información sobre Biotecnología, Biblioteca Nacional de Medicina, Bethesda, MD. Disponible en:http://omim.org/entry/208900 . Consultado el 24 de octubre de 2012.3.
Buoni S, Zannolli R, L Sorrentino, Fois A. La betametasona y la mejora de los síntomas neurológicos en la ataxia telangiectasia . Arco Neurol 2006; 63 :. 1469-1482 [ PubMed ]4.
Broccoletti T, E Del Giudice, Cirillo E, et al. Eficacia de betametasona en dosis muy baja en los síntomas neurológicos en la ataxia-telangiectasia . Eur J Neurol 2011; 18 :. 564-570 [ PubMed ]5.
Zannolli R, S Buoni, Betti G, et al. Un ensayo aleatorizado de betametasona oral para reducir los síntomas de la ataxia en la ataxia telangiectasia . Mov Disorders, 2012; 27 :. 1312-1316 [ PubMed ]6.
. Chessa L, V Leuzzi, Plebani A, et al infusión intra-eritrocitos de dexametasona reduce los síntomas neurológicos en pacientes con ataxia teleangiectasia: resultados de un ensayo de fase 2 . Orphanet J Rare Dis 2014; 9 : 5. [ Artículo libre PMC ] [ PubMed ]7.
Magnani M, L Rossi, D'Ascenzo M, Panzani I, L Bigi, Zanella A. ingeniería de eritrocitos para la administración de fármacos y la orientación . Biotechnol Appl Biochem 1998; 28 : 1-6. [ PubMed ]8.
Trouillas P, T Takayanagi, Hallett M, et al. Cooperative Ataxia Escala de Evaluación Internacional para la evaluación farmacológica del síndrome cerebeloso. El Comité Ataxia Neurofarmacología de la Federación Mundial de Neurología . J Neurol Sci 1997; 145 : 205-211. [ PubMed ]9.
Van Duijn G, Dijkxhoorn Y, Noens I, E Scholte, van Berckelaer-Onnes I. Vineland Screener 0-12 años versión de la investigación (NL). La construcción de un instrumento de cribado para evaluar el comportamiento de adaptación . Int J Métodos Psychiatr Res 2009; 18 :. 110-117 [ PubMed ]10.
Moxley RT, III, Ashwal S, Pandya S, et al. ; Normas de Calidad Subcomité de la Academia Americana de Neurología, Comité de Práctica de la Child Neurology Sociedad. Parámetro de la práctica: el tratamiento con corticosteroides de la distrofia de Duchenne: informe del Subcomité de Normas de Calidad de la Academia Americana de Neurología y el Comité de Práctica de la Sociedad de Neurología Infantil .Neurología 2005; 64 :. 13-20 [ PubMed ]